灰から炭酸カリウムを作る|灰汁で作るカリウム石けん その③
2017/03/02
この話に登場する化学物質たち
みんな名前が似ているため、かえって記号の方がわかりやすかったりします。
炭酸カリウム(K2CO3)
→草木灰に少量含まれる物質。灰汁を煮詰めて取り出す。pH10-11の弱アルカリ。
これとCa(OH)2を反応させてKOHを作るのが目標。
水酸化カリウム(KOH )
→別名苛性カリ。pH14の強アルカリ。石けん作りには欠かせないアルカリ剤のひとつ。
最終的にこの物質を作るのが目標。
水酸化カルシウム(Ca(OH)2)
→別名消石灰。食品乾燥剤の生石灰を消化して作る予定。K2CO3と反応させてKOH にする。
前回のおわりに悩んでいた「炭酸カリウム(K2CO3) 作り」ですが、5時間かけて5グラムずつ×9セットというのは耐え難いので、別の方法で水酸化カリウム(KOH)を入手することにしようかと思ったんですけど・・・
注:なぜ5グラムずつしか作れないのかと言いますと、鍋の大きさの問題です。
試してみようかなーと思った新たな水酸化カリウムの入手方法は、以下のような仕組みです。
用意するもの
・下に穴を開けたバケツ(または大きめのコットン袋)
・バケツを使う場合は、フィルターとして藁、砂利、小枝などを用意
・雨水
・出来上がった水溶液を受けるためのバケツ
・草木灰
・水酸化カルシウム(消石灰)
フィルタリングする容器に下から順番に、砂利・小枝・藁(コットン袋を使うなら不要)→水酸化カルシウム→草木灰と入れていき、上から雨水を流し入れます。
すると下から出てくる水溶液は、水酸化カリウム(KOH)を含むというものです。
「この方法なら一気に沢山作れる!」と単純に考えてしまったんですが、取り出した水溶液に含まれる水酸化カリウム(KOH)の量というのは結局、もともと灰汁に含まれている炭酸カリウム(K2CO3)の量が変わらない以上、今までやっていた方法と大差ないということに気がつきました。
たとえ取れた水溶液を結晶化させずにそのまま石けん作りに使おうとしても、鹸化価というものがあるので、満足に反応させるにはおそらく大量の水溶液が必要になってしまいます。
※鹸化価: 油脂1g に対して必要な水酸化カリウムのmgのこと。
それに炭酸カリウムと水酸化カルシウムがしっかりと反応するのかも不安です。
そこで石けん作りに使用する予定の油脂の量を減らすことにしました。
そうすれば、使用する水酸化カリウム(KOH)も少なくて済むという算段なのです。
そういうわけで、作る炭酸カリウム(K2CO3)の目標量を50グラム→15グラムとしました。
すでに7グラム作ってありますので、あと8グラム作ればいいのです!
せっかく石けんを作るというのに量が少ないというのも、もったいない気がしますけど・・・。
そして一度に作る炭酸カリウムの量を増やすために、前回の工程(4)と(5)において、「灰汁を沸騰させて水分を飛ばしながら、飛んだ分だけ灰汁を加えていく」という追加法を思いつきました。
そんなふうにして一度に13グラムの炭酸カリウム(K2CO3)を作ることができました。




合計すると20グラム!
やったよー!!
5グラムしか作れなかったものが、追加法で13グラムにまで増えました。
灰を水につけたまま一晩寝かせた灰汁を使ったのもよかったのかもしれません。
さて次に、炭酸カリウム(K2CO3)と水酸化カルシウム(Ca(OH)2)を反応させて水酸化カリウム(KOH)を作ります。
と、そのまえに生石灰から消石灰(水酸化カルシウム)を作ろうと思います。
ウチにある食品乾燥剤を集めてきました。

これに水をかけて消化するとできあがるのが、水酸化カルシウムです。
そして水酸化カルシウムと炭酸カリウムを混ぜて水に溶かしたものを加熱し、水分を飛ばして最後に残った物体が、水酸化カリウムを含んでいる!!はずです。
化学反応としては、こんな感じです。
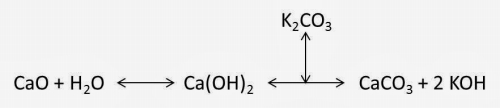
待望の水酸化カリウム(KOH)が手に入ると同時に炭酸カルシウムも手に入ることになりますが・・・。
全部を反応させる前に、試しに少しだけ反応させてpHを測ってみましょうかね・・・。

自作の炭酸カリウムは大変貴重なパウダーなのでほんの少しだけ。
水を加えてpHを測ってみます。

やはりpH10程度。
ここに生石灰を加えてよく混ぜました。

消化する際に発熱するとのことでしたが「?」という状態です。
もしかして反応していない・・・??
「どうせ水に入れるんだから、前もって消化しなくてもいいのでは?」と思って、生石灰を直接溶液に加えたのがわるかったのでしょうか・・・
よくわかりません。
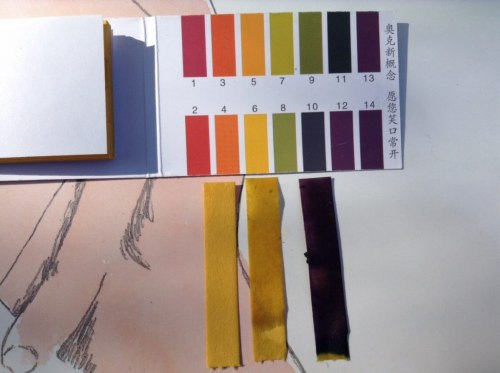
とにかくpHを測ってみますと

おお、pH13くらい??
と、ここで大事なことを忘れていました。
そういえば生石灰ってもともとpHはいくつなのか?ということです。
計測してみました。

pH13くらい。(右の試験紙は生石灰水溶液、左は生石灰+炭酸カリウム水溶液)
うーん、これでは炭酸カリウムと炭酸カルシウムが反応した結果、pHが高くなったのかどうかわからなくなってしまいました・・・。
でも、こうなったら化学反応式を信じるしかありません。
不安でいっぱいですが、次回はいよいよ石けんを作ります!!
おまけの灰のはなし
「針葉樹の灰よりも広葉樹の灰のほうがより炭酸カリウムを含んでいる」という説がありますが、それは本当なのでしょうか。
1、針葉樹の多くは「裸子植物」に分類されます。広葉樹の多くは「被子植物」です。
裸子植物のカリウム含有量は被子植物よりも少ないというレポートがあります。
おおまかに植物のカリウム含有量を比較してみますと、コケ類 < 羊歯類 < 裸子植物 < 被子植物となります。
2、「針葉樹は広葉樹に比べてヤニが多いので、より高温で燃焼する」
とよく言われますが、900度を超えると大半の炭酸カリウムは気化してしまうとの研究結果があります。
例えば針葉樹が950 度、広葉樹が700度で燃焼するとすれば、針葉樹の灰に含まれる炭酸カリウムは広葉樹の灰よりも少ないということになります。
(1,000度以上の高温になる焼物の窯には針葉樹の松が使われます)
ただし、900度というのは相当な高温です。通常は滅多に達することはないでしょう。
というわけで、針葉樹の灰よりも、広葉樹の灰(900度以下で燃焼させたものに限る)のほうがより炭酸カリウムを含んでいるといえます。
ちなみに今回使った灰は、針葉樹と広葉樹が混ざったものでした。