灰汁を使って石けんをつくる その②|灰から炭酸カリウムを取り出す方法
2017/03/07
灰シリーズのごあんない
・薪ストーブの灰で灰汁をつくる
・灰汁の使い道と草木灰で食器を洗う
・草木灰の灰汁でつくる石鹸(失敗編)
・灰汁を使って作るプリミティブな石けん(はじめに)
・灰汁を使って石けんをつくる その②|灰から炭酸カリウムを取り出す
・灰汁で作るカリウム石けん その③|灰から炭酸カリウムを作る
まずは灰から炭酸カリウムを取り出します。
その1「灰汁を使って作るプリミティブな石けん(はじめに)」はこちらから
その前に「灰」とは?
木や木炭が燃えたあとに残る灰は、さまざまな非可燃性、非揮発性の無機物の混合物です。
燃焼ガス中に存在するCO2や、無機物の多くはカーボネイトに変化しますし、灰の中にはもしかすると焼けた土も含まれるかもしれません。
つまり灰のなかには主に炭酸ナトリウム・炭酸カリウム、そして塩化ナトリウム・塩化カリウム、シリカ類、炭酸カルシウムが含まれていると考えることができます。
それを踏まえて灰からなるべく炭酸カリウムだけを取り出そうと思います。
用意するもの
・草木灰
・雨水
・2リットルのペットボトル(バケツを使っても○)
・素焼きのツボまたはガラスやステンレスのナベ(アルミはダメ)
・混ぜるためのスプーン
・お酢またはクエン酸(使った器具は全て中和してから洗います)
1、ペットボトルまたはバケツの1/3くらいまで灰を入れ、残りの部分を雨水で満たします。
2、キャップをしめて、よく振ってかく拌し、そのまま1日放置します。


攪拌すると溶液全体が灰色に濁りましたが、10分も経たないうちに固形物は沈殿し上澄みはベージュがかった透明の液体になりました。

この状態でとりあえずpHを測ってみます。

この試験紙はアマゾンで送料込み88円で買ったものです。
商品説明をよく読まなかったので、まさか中国から発送だなんて知らなくて、注文してから届くまで2週間ほどかかりましたし、開けてびっくりの小ささでした。
ちぎって使う紙マッチの箱くらい。
試験紙自体が黄色すぎて、微妙な色の変化がわかるのか不安ですけれど、とにかくやってみます。
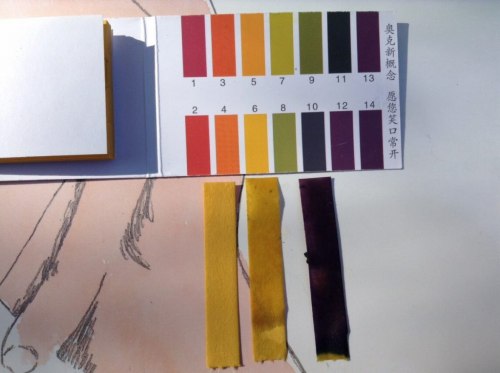
試験紙が鮮やかに色づき、凡そpH10を示しました。
まんなかの試験紙は雨水に浸したものでpH6くらい?
左の試験紙は何も浸していないものです。
当初ペットボトルを1日放置するつもりでしたが、pH的にすでに充分カリウム等がとけていると思ったので、固形物が沈殿してから2時間ほど経ったのちに次の工程に移りました。(大丈夫??)
3、不溶解性のシリカ類や炭酸カルシウムは溶けずに底に溜まります。上に浮かんでいるのは炭です。
これらの固形物が入らないように注意しながら、液体だけを他の容器に移します。

耐熱ボウルに上澄みだけを移しました。
TIPS
pH試験紙がない場合には、生のタマゴを使って大体を知ることができるそうです。
タマゴを溶液に入れて、どのくらい浮かぶかで判定します。
・タマゴが少し顔を出すくらいなら、ちょうどいい。
・沈んでしまうのは、アルカリが弱すぎる。
ということみたいですが、ためしにタマゴを入れてみたところ、すとんと下まで沈んでいきました。
どうやらpH10程度では、タマゴは沈むようです。

そういえば確かタマゴの鮮度を確認するのに水に浮かぶかどうかで判定する方法がありました。
使用するタマゴによっても結果が変わる気がするので、どうせなら紫キャベツなどで試験液を作ったほうが確実な気がします。
そもそも炭酸カリウムのpH程度でタマゴが浮かぶのでしょうか・・・?
(古いタマゴだったら浮かぶかも?)
ちなみにタマゴが沈んでしまった場合はアルカリを強くするために、作った灰汁を使って灰汁を作り直す(雨水のかわりに灰汁を使う)か、水溶液を煮詰めて濃くする方法があります。
前回書いたとおり、一般的にカリウムの飽和溶液のpHは10〜11程度とされていますので、アルカリを強くする方法は灰汁のpHがそれ以下の場合に有効なんだと思います。
ちょうどこれからカリウムを取り出すために灰汁を煮詰めていきますので、そのときにpHに変化があるのか計測してみようと思います。
4、取り出した溶液には、溶解性の炭酸ナトリウム・炭酸カリウムや塩化ナトリウム・塩化カリウムが溶けています。
溶液を加熱して沸騰させます。
ウチにはステンレスの鍋がありませんので今回パイレックスの耐熱ボウルを使いましたが、パイレックスのサイトで確認しましたら、直火はダメとのこと。
間接的ならいいかと、鉄のフライパンを敷いた上にパイレックスを置いて加熱することに。

しかしこの選択が後に悲劇を生むのです・・・。
ちなみに熱源は燃費の良い灯油コンロのトヨコンロです。
5、沸騰してしばらくすると、沈殿物が生じます。
これはほとんど塩化ナトリウム・塩化カリウムです。
加熱を始めて30分後。
沸騰こそしていませんが、ボウルの底一面に灰白の細かい粒が沈殿していました。

6、ここから残っている水溶液が半分くらいになるまで、さらに沸騰させます。
加熱1時間後、突然弾けるような音が!
パイレックスにヒビが入って、漏れた溶液が熱いフライパンに触れた音でした・・・。
仕方ないのでこれで加熱を終えようかとも思いましたが、しかしまだ蒸発が足りないので、急遽第2の鉄のフライパン「リバーライト」をきれいに洗って、そこに沈殿物以外の水溶液を移して加熱を続けることにしました。
すると直ぐに沸騰しはじめるリバーライト。
さすが直火は強い!
7、沈殿物を残して、水溶液を他の容器に移します。
この水溶液には、炭酸ナトリウム・炭酸カリウムが溶けています。

さて、この時点で水溶液は当初の半分の量になっていますので、先の疑問「煮詰めるとpHはどうなる??」を確かめてみました。

pH10程度で変化なし。
8、取り出した水溶液を室温になるまで冷まします。
炭酸ナトリウムは炭酸カリウムよりも若干溶けにくい性質なので、炭酸ナトリウムが先に固形になって沈殿します。
そうしたら、沈殿物をそのままにして水溶液だけを慎重に他の容器に移します。
水溶液の温度が25度程度になったときにフライパンを傾けてみましたら、確かに白い沈殿物ができていました。
その沈殿物が入らないように別の容器に水溶液を移しました。

そこで気になったのが、水溶液の色です。

茶色い・・・。
リバーライトに固着していた「コゲ」が溶けたものだと思いますが、大丈夫なんでしょうか?
取り出せた水溶液はおそらく100mlほどです。
少ない・・・。
9、取り出した水溶液に溶けているのはほとんど炭酸カリウムだと予想されるので、水溶液中の炭酸カリウムが粉末になるまで加熱して水分を飛ばします。
火をつけてすぐにパチパチと爆ぜる音が聞こえはじめ、油断していたらあっという間にこんな状態に。

コンロの周りにも飛んで汚い・・・。

プラスチックスプーンで粉末を集めようとしましたが、全然とれません。
そこでステンレススプーンの柄を使って削ること15分、なんとか8割がた取ることができました。
すべての工程の中で、この炭酸カリウム粉末をこそぎ落とす作業が一番大変でした。
コンロに飛んだものを素手で集めていましたら、指がヒリヒリしてきたのでお酢で中和しました。
素手は厳禁です!
沸騰させているときに発生する蒸気も危険なので屋外で作業することをオススメします。
わたしは室内で作業していて吐き気を催したので外に移動しました。
マスク着用も忘れずに。
10、炭酸カリウム!?ができたー!

20リットルのペットボトルで作りましたら、約2グラムの炭酸カリウムができました。
参考までに、かかった時間は5時間です。
さて、2グラムでは全然足りないので、面倒でも量産しようと思います。
追記 その1
2度目に炭酸カリウムを作ったときには鉄のフライパンを使うのをやめました。
すると(8)の時点で出来上がった水溶液の色は茶色ではなくて、うっすらベージュ色した透明の液体になりました。
やっぱり茶色の正体はフライパンに付着していたコゲだったみたいです。
追記 その2
最後の工程、炭酸カリウムが粉末になるまで水分を飛ばす段になって、もう一度pHを測ってみましたら、pH10よりもpH11寄りの色になりました。(いままではどちらとも言えない色だった)

さらに結晶化寸前の時点も測ってみました。

やっぱりpH11が限界のようです。
試験紙が乾いたらキラキラした結晶が出てきた。

さきほどは、この方法で炭酸カリウムをたくさん作るぞー!と意気込んでいましたが、第2回目の作業を終えて手に入れた炭酸カリウムの量を見たとたん、これは無理な野望なのではないかと思うに至りました。
2回目は、前回の3倍の量の灰汁を煮詰めましたが、出来た炭酸カリウムはたったの5グラム。
前回と合わせても7グラムしかありません。
「50グラムくらい作ろうかなー」なんて考えていましたけれど、あと9回も繰り返す気力が湧きません・・・!!
ここでがんばるのか、代替え案を探すのか!!






